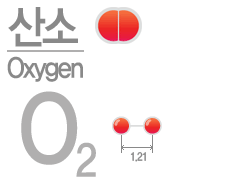
산소(Oxygen)
산소는 공기중에 78%인 질소 다음으로 많은 약 21%이며 16%이하로 떨어지게되면 호흡이 힘들어지게 된다. 산소는 모든 생명체에 필수요소이며 산소자체는 불연성이지만 가연성 물질과 반응하게되면 강한 산화반응을 일으키는 조연성물질이다. 끓는점(액화 온도)은 -183℃이며 공기를 빨아들여 불순물을 거른후에 공기의 단열팽창을 이용하여 얻는 방식을 많이 사용한다.
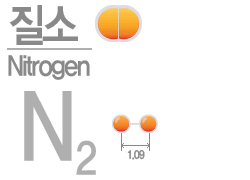
질소(Nitrogen)
질소는 공기중에 78%를 차지하고 있으며 무색, 무미, 무취로 불활성 및 불연성이다. 라틴어 초석(nitrum)과 그리스어 생성한다(gennao)가 합쳐져서 질소 Nitrogen이 생겼다. 끓는점(액화온도)은 -196℃이며 질소는 대기뿐만 아니라 바다, 암석 등에도 넓게 있다. 또한 질산, 암모니아, 단백질, 핵산 등의 화합물에도 있다. 생산방식은 단열팽창을 이용하여 주로 생산한다.
아르곤(Argon)
매우 안정하므로 전구나 용접 등에 사용하는 아르곤은 공기중에 질소, 산소 다음으로 많은 약 0.93%를 차지하고 있다. 무색, 무미, 무취이며 불활성, 불연성이다. 끓는 점은 약 -186℃. 생산방식은 질소, 산소와 마찬가지로 단열팽창을 이용하여 생산한다. 대부분의 아르곤은 K의 붕괴에 의해 만들어진 것이다.
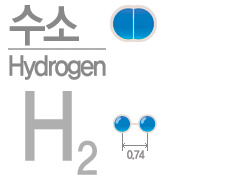
수소(Hydrogen)
지구에 있는 가스중 가장 가볍고 무색, 무미 무취다. 확산이 빠르며 가연성이다. 수소는 연소 후 물만 만들어지고 오염물질이 발생하지 않아 미래의 청정에너지로 각광을 받고 있다.
이산화탄소(Carbon Dioxide)
무색, 무취의 불연성 가스로 낮은 압력에서도 쉽게 액화가 가능하며 이를 더 압축하면 드라이아이스가 된다. 알코올 발효시 부산물로서 얻는 등 주로 부산물로 생산한다.
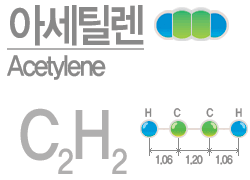
아세틸렌(Acetylene)
무색, 무취의 기체이지만, 카바이드에서 만들면 냄새가 나는 것은 불순물이 섞였기 때문이다. 공기 또는 산소와의 혼합물은 폭발하기 쉽기 때문에 취급할 때 주의가 필요하다. 아세톤에는 잘 녹기때문에 아세톤을 규조토에 흡수시켜 가압하여 녹이고 운반한다.
혼합가스(Mixed Gases)
산업이 다양화 및 고도화되면서 두가지 이상의 고순도 가스를 적절하게 섞어서 사용해야하는 경우가 늘었으며 다양한 분야에서 사용하고 있다.

용도
레이저, 특수용접, 방사능 측정, 특수분석기기 등.
특수가스(Special Gases)

반도체용 특수가스, 초고순도 순수가스, 표준가스 등